2024.12.12
5242
热点资讯 | NEWS
近日,在复旦大学附属儿科医院耳鼻咽喉头颈外科和浙江大学医学院附属儿童医院耳鼻咽喉头颈外科开展的“布地奈德混悬液经鼻雾化治疗儿童腺样体肥大疗效及安全性研究”的随机对照研究成果,分别在《中国实用儿科杂志》和《临床耳鼻咽喉头颈外科杂志》上发布。《中国实用儿科杂志》为北大核心、科技核心、中国科学引文数据库来源(CSCD)核心期刊,是儿科领域的专业期刊,创刊30多年来,影响广泛,发行量居国内儿科期刊领域杂志首位,目前主要发表儿科领域的新成果、新技术、新进展等。《临床耳鼻咽喉头颈外科杂志》被多个权威数据库收录,包括北大核心期刊、CSCD期刊、我国高质量科技期刊分级目录T2类期刊,并被PubMed Central(PMC)、Medline、CA、Scopus、WPRIM等重要数据库收录。
这项研究首次探索了高渗/生理性海水鼻腔清洗联合吸入用布地奈德混悬液经鼻雾化治疗儿童腺样体肥大的疗效及安全性,并探索了吸入用布地奈德混悬液的适用剂量。研究结果显示该治疗方案既能有效改善鼻塞、打鼾等临床症状,又能减轻腺样体肥大程度,且药物安全性良好, 给药方式舒适度高, 儿童易于接受。这些研究结果将逐步转化到实际的临床工作中,为腺样体肥大患儿提供一种安全、可持续缓解腺样体上气道阻塞的治疗方案,具有普及性强,依从性高的特点,且可以在临床中替代手术治疗的治疗方案,该方案具有临床推广价值,可以帮助更多腺样体肥大患儿获益。
临床背景
腺样体肥大是一种常见的儿童疾病, 其发病率在儿童中高达34%[1]。由于腺样体异常增大,堵塞鼻咽部,导致上气道阻塞,从而引发一系列临床症状,并产生阻塞性睡眠呼吸暂停综合征、分泌性中耳炎、鼻炎、鼻窦炎、颔面部发育畸形(腺样体面容)、神经认知损伤等严重并发症[2.3]。长此以往,对儿童的生长发育造成严重的危害。目前,药物和手术是治疗小儿腺样体肥大的主要方法[4]。腺样体切除术是临床上治疗腺样体肥大的常见治疗方法,但腺样体切除术因考虑到术后出血、发热等并发症,所以至今尚存争议[5]。因此寻找一种安全有效的非手术治疗方法是非常必要的。经临床实践证明,鼻腔盐水冲洗和鼻用糖皮质激素有较好的治疗效果。鼻腔盐水冲洗有助于清除鼻腔内的过敏原和炎性分泌物并减轻鼻黏膜水肿,布地奈德是儿童常用的吸入及鼻用糖皮质激素, 具有良好的安全性并能够有效缓解鼻腔炎症反应。相关研究发现,雾化吸入布地奈德可有效改善腺样体肥大患儿的症状,并缩短病程,显著降低腺样体切除术率[6]。因此,本研究旨在通过随机对照设计,比较高渗/生理性海水鼻腔清洗联合吸入用布地奈德混悬液经鼻雾化治疗儿童腺样体肥大的疗效及安全性,并探索了吸入用布地奈德混悬液的适用剂量,为临床应用提供指导性证据。
试验设计
本试验采用随机、开放、多组比较设计,入选130例受试者(预试验组10例,试验组120例),患者年龄为2岁≤年龄<5岁(复旦大学附属儿科医院-复儿);5岁≤年龄<8岁(浙江大学医学院附属儿童医院-浙儿),所有患儿均有3个月及以上的临床症状(如鼻塞、咳嗽、夜间睡眠打鼾等),且符合临床腺样体肥大诊断标准,并经鼻内镜检查证实腺样体阻塞后鼻孔Ⅱ-Ⅲ度阻塞,且经鼻咽侧位X线显示腺体最大厚度与鼻咽腔前后径距离之比(A/N)值,0.61≤A/N≤0.80。
治疗方案
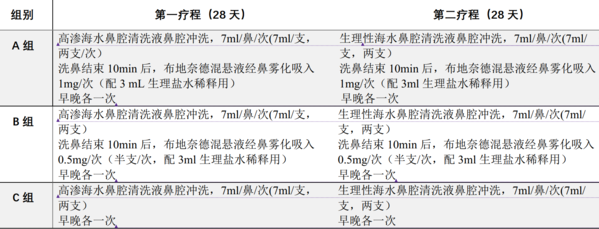
研究共分为2个疗程, 每个疗程分别为28天。患儿被随机分配至布地奈德高剂量组(A 组: 布地奈德1 mg/次+海水鼻腔冲洗)、布地奈德低剂量组(B 组: 布地奈德0.5 mg/次+海水鼻腔冲洗) 、对照组(C 组: 海水鼻腔冲洗)具体的治疗方案, 见下表:
试验用药物及辅助器械选择
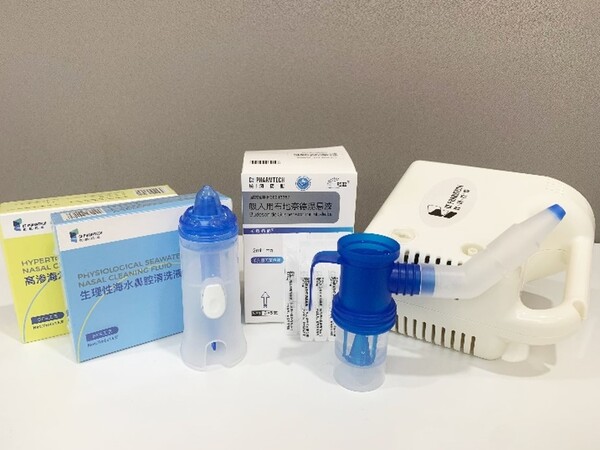
(1)吸入用布地奈德混悬液(商品名:畅起®,长风药业股份有限公司,规格:2 mL:1mg,批准文号:国药准字H20213357);
(2)高渗海水鼻腔清洗液(长风药业股份有限公司,规格:7 mL,医疗器械注册证编号:苏械注准 20202141291);
(3)生理性海水鼻腔清洗液(长风药业股份有限公司,规格:7 mL,医疗器械注册证编号:苏械注准 20202141292);
(4)医用压缩式雾化器(长风药业股份有限公司,医疗器械注册证编号:湘械注准 20202081601);
(5)医用冲洗头(长风药业股份有限公司,医疗器械注册证编号:苏镇械备20180004)。
研究结果1(2岁≤年龄<5岁,n=54)
复儿的试验数据结果采用SPSS 26.0进行分析。采用Shapiro-Wilk法进行正态检验,符合正态分布的数据采用均数±标准差(x±s)表示,并采用单因素方差分析(ANOVA)对 3 组进行比较,其中方差齐性数据的事后比较(post hoc)采用 LSD 法,方差不齐数据的事后比较采用塔姆黑尼法(tamhane)。
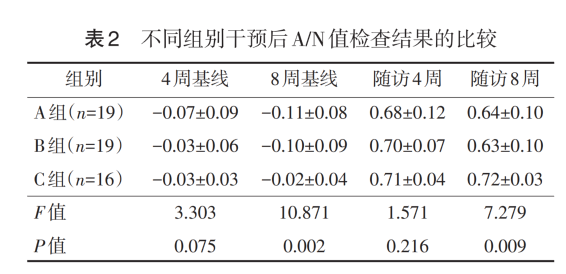
本研究的主要结局指标为鼻咽侧位片 A/N 值的8周基线差值,治疗8周后,共有17例患儿A/N值恢复到正常范围,方差分析的结果显示,经干预后,经事后比较检验,A 组与 C 组 A/N 实测值(P=0.010)和较基线变化值(P=0.001)在首次给药后 8周时均有统计学差异;B 组与 C 组 A/N 实测值(P=0.003)和较基线变化值(P=0.009)在首次给药后 8周时均有统计学差异,具体见下表。说明经过两个疗程的治疗后对疾病控制有明显的作用。
随着干预时间的增加,三组治疗后视觉模拟量表(VAS)各症状评分均随着治疗时间的延长呈下降趋势,干预8周后,A、B组患儿的VAS评分和C组相比均有显著降低(P<0.05),A组和B组的VAS总分之间差异无统计学意义(P=0.844)。结果表明A、B组患儿经过治疗后的鼻塞、打鼾、张口呼吸和咳嗽等症状均有明显改善(P<0.01),其中A组患儿改善程度最大。
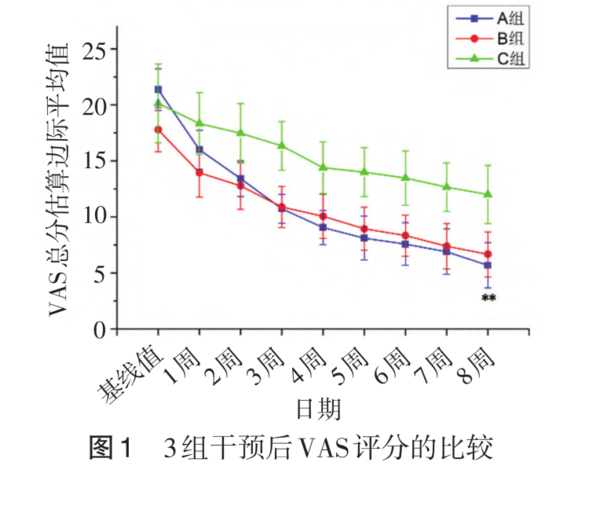
在整个试验中,其中与试验药品相关(包括肯定有关、很可能有关、可能有关)的不良事件(TRAE)的总发生率为 13.3%,A、B、C 组分别发生4例、3例、2例,3组患儿发生TRAEs的发生率均较低。所有 TRAEs 均属于轻度,未经干预患儿可自行恢复,在整个研究期间,没有发生与试验用药品相关的严重不良事件,也没有患儿因药物相关的不良事件而退出研究,该试验药物安全性和耐受性良好。
研究结果2(5岁≤年龄<8岁,n=54)
浙儿的数据结果使用SPSS 26.0进行分析。采用Shapiro-Wilk法进行正态检验, 符合正态分布的数据采用X±S 表示, 主要结局为鼻咽侧位片 A/N值的8周基线差值采用单因素方差分析 (ANOVA) 进行组间比较, 方差齐性数据事后比较(POST HOC)采用LSD法, 方差不齐数据采用塔姆黑尼法(tamhane)。
研究结果显示,3 组腺样体A/N值的4周基线差值比较差异无统计学意义, 腺样体 A/N 值的8 周基线差值比较差异有统计学意义(F =7.981 ,P =0.001) , 其中, 经事后比较检验,A组与B组(P <0.001 )、A组与C组(P =0.022) 比较差异均有统计学意义,B组与C组比较差异无统计学意义(P =0.137)。经过8周治疗,A组腺样体体积前后改变量最为明显,与其他2 组比较存在差异,B组和C组腺样体体积前后改变量无明显差异。

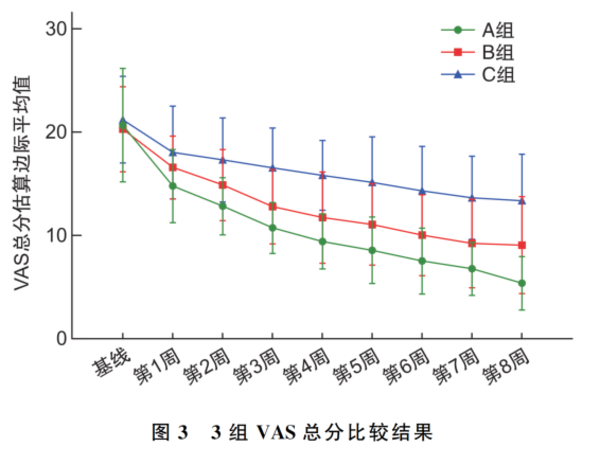
随着干预时间的增加,三组治疗后视觉模拟量表(VAS)各症状评分均随着治疗时间的延长呈下降趋势,8 周后, 事后分析的两两比较发现, A、B 组的 VAS总分比较差异有统计学意义 (P =0.026 ) , A 组VAS 总分的改善程度较B 组高;A、B 组的 VAS 总分与 C 组比较差异均有统计学意义(P <0.05 )。因此, 3 组经8周干预后, A 组的治疗方案对患儿的鼻塞、打鼾、张口呼吸和咳嗽等症状的改善程度最大, 其次是 B 组。
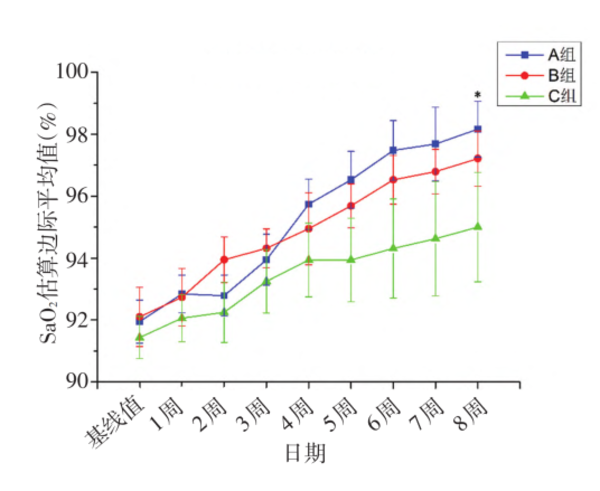
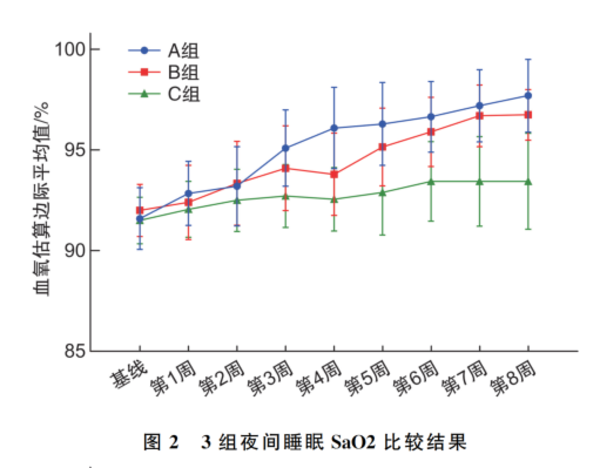
3 组患儿随着治疗时间的增加,夜间睡眠血氧饱和度(SaO2)逐渐上升(P<0.01), A 组的SaO2 和 C 组比较有显著改善(P<0.01)同时研究结果表明, 高浓度的布地奈德混悬液经鼻雾化在改善腺样体肥大的患儿的夜间睡眠 SaO2 方面比低浓度更为有效。
本研究发现常见不良反应为感冒(13.30%)、咳嗽(8.33%)、流涕(5.00%)、鼻出血(5.00%),3组不良事件及药物不良反应发生率无明显差异, 不同剂量布地奈德混悬液经鼻雾化治疗腺样体肥大患儿与对照组比较, 不会增加不良反应的发生, 布地奈德混悬液经鼻雾化的药物安全性良好。
结论
综上所述,高渗/生理性海水鼻腔清洗联合布地奈德混悬液经鼻雾化治疗儿童腺样体肥大可以有效控制患儿症状、改善患儿的生活质量、降低部分患儿腺样体肥大程度,提高夜间睡眠血氧饱和度,有助于整体病情的控制,并且在整个研究期间,没有发生与试验用药品相关的严重不良事件,该试验药物在治疗期间安全性和耐受性良好,具有一定的临床推广价值,可以为患儿带来临床获益。
【参考文献】
[1] Pereira L, MonyrorJ, Almeida FT, et al. Prevalence of adenoid hypertrophy: A systematic review and meta analysis[J]. Sleep Med Rev,2018,38:101-112.
[2] Liu X,Jiang Z,Xiao Z,et al. Meta- analysis of Chinese medicine in the treatment of adenoidal hypertrophy inchildren[J]. Eur Arch Otorhinolaryngol,2019,276(1):203-208.
[3]Wang P,Kong W,Shan Y. The efficacy and safety of Chinese herbal compound or combined with western medicine for pediatric adenoidal hypertrophy:a protocol for systematic review and meta-analysis[J]. Medicine (Baltimore),2020,99(36):22023.
[4] Schupper AJ,Nation J,Pransky S. Adenoidectomy in children:what is the evidence and what is its role? [J]. Curr Otorhinolaryngol Rep,2018,6(1):64-73.
[5]Marcus CL. A randomized trial of adenotonsillectomy for childhood sleep apnea[J]. N Engl J Med, 2013.368(25):2366-2376.
[6] 罗双伟. 小儿急性化脓性扁桃体炎合并腺样体肥大采取布地奈德雾化吸入治疗疗效观察[J]. 中国现代药物应用, 2020, 14(7):172-173.
[7]Criscuoli G,D’Amora S,Ripa G,et al. Frequency of surgery among children who have adenotonsillar hypertrophy and improve after treatment with nasal beclomethasone[J]. Pediatrics, 2003, 111: 236-238.